Ο μη μυοδιηθητικός καρκίνος της ουροδόχου κύστης (non–muscle–invasive bladder cancer, NMIBC) αποτελεί το 70% περίπου των νεοδιαγνωσθέντων περιστατικών με κακοήθεια της ουροδόχου κύστης. Θέτει σημαντικές κλινικές προκλήσεις λόγω των υψηλών ποσοστών υποτροπής και εξέλιξης. Στο πλαίσιο της ετερογένειας της νόσου, τα τελευταία χρόνια η υποομάδα υψηλού κινδύνου (High Risk, HR) έτυχε ιδιαίτερης προσοχής.
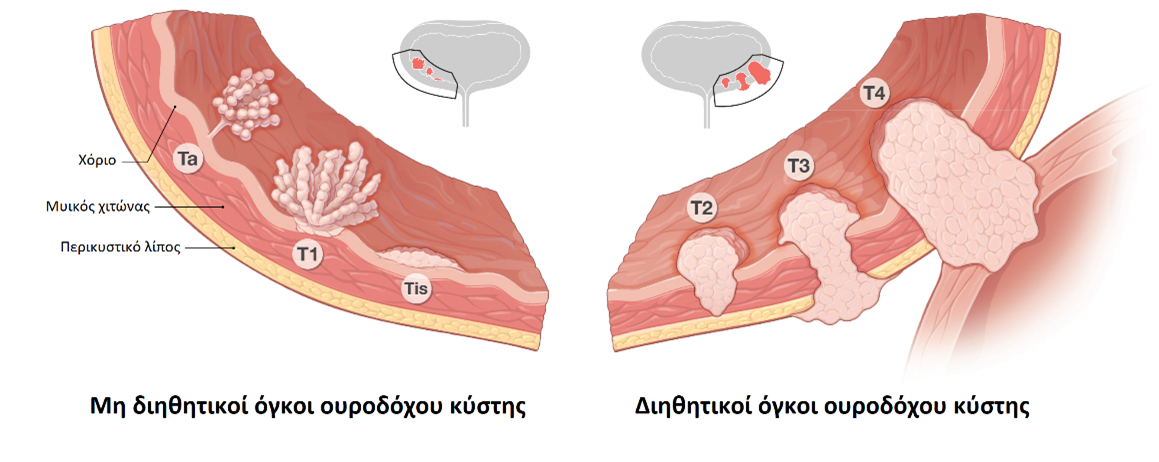
Εξατομικευμένη μοριακή θεραπεία σε υψηλού κινδύνου ασθενείς με καρκίνο ουροδόχου κύστης
Παρά το καθιερωμένο πρότυπο φροντίδας (standard of care, SOC), που αντιπροσωπεύεται από διουρηθρική εκτομή του όγκου (TUR-BT) ακολουθούμενη από ένα σχήμα συντήρησης επικουρικής ενδοκυστικής ανοσοθεραπείας με Bacillus Calmette–Guérin (BCG), η αποτυχία της θεραπείας εξακολουθεί να αποτελεί σημαντική ανησυχία.
Περίπου έως και το 40% των ασθενών εμφανίζουν υποτροπή εντός ενός έτους και έως και 20% τελικά εξελίσσονται σε μυοδιηθητικό καρκίνο της ουροδόχου κύστης (muscle-invasive bladder cancer, MIBC). Παραδοσιακά, η ριζική κυστεκτομή ήταν το πρότυπο για τη νόσο που δεν ανταποκρίνεται στο BCG, αν και επηρεάζει σημαντικά την ποιότητα ζωής και εμφανίζει σημαντική νοσηρότητα.
Οι πρόσφατες εξελίξεις έχουν επικεντρωθεί σε θεραπείες διατήρησης της ουροδόχου κύστης που αξιοποιούν:
- αναστολείς σημείων ελέγχου του ανοσοποιητικού
- νέα συστήματα χορήγησης φαρμάκων
- στοχευμένους μοριακούς παράγοντες
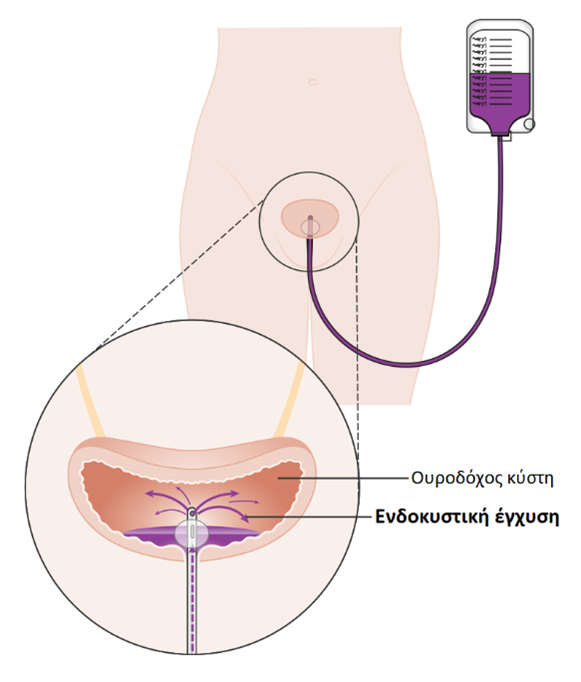
Επικουρική ενδοκυστική ανοσοθεραπεία με Bacillus Calmette–Guérin (BCG)
Σύμφωνα με τις κατευθυντήριες οδηγίες της Ευρωπαϊκής Ουρολογικής Εταιρείας (EAU), η νόσος που δεν ανταποκρίνεται στο BCG περιλαμβάνει όλους τους ανθεκτικούς στο BCG όγκους, που ορίζονται από την επιμονή ή την εξέλιξη των υψηλού βαθμού βλαβών εντός έξι μηνών από την έναρξη ή κατά τη διάρκεια της θεραπείας συντήρησης BCG, και τους πρώιμους υποτροπιάζοντες όγκους, που χαρακτηρίζονται από υψηλού βαθμού υποτροπή εντός έξι μηνών μετά την ολοκλήρωση της θεραπείας συντήρησης.
Αν και το BCG έχει χρησιμοποιηθεί στη διαχείριση του καρκίνου της ουροδόχου κύστης για αρκετές δεκαετίες, ο ακριβής μηχανισμός δράσης του παραμένει ατελώς διευκρινισμένος. Οι βιολογικοί μηχανισμοί που κρύβονται πίσω από αυτή τη μη ανταπόκριση είναι ελάχιστα κατανοητοί και πιθανώς πολυπαραγοντικοί. Περιλαμβάνουν πολύπλοκες αλληλεπιδράσεις μικροπεριβάλλοντος όγκου-ουροδόχου κύστης και ανοσολογικούς παράγοντες του ξενιστή.
Δεδομένου του σημαντικού κινδύνου υποτροπής και εξέλιξης του όγκου, η πρώιμη ριζική κυστεκτομή προτείνεται ως SOC για ασθενείς με NMIBC που δεν ανταποκρίνονται στο BCG. Τα ποσοστά επιβίωσης ειδικά για τον καρκίνο (cancer–specific survival, CSS) μετά από κυστεκτομή υπερβαίνουν το 80%. Ωστόσο, ένα σημαντικό ποσοστό ασθενών αρνείται τη θεραπεία λόγω:
- ανησυχιών σχετικά με την περιεγχειρητική νοσηρότητα και
- τον επακόλουθο αντίκτυπο στην ποιότητα ζωής (QoL).
Ως αποτέλεσμα, αναπτύσσονται πρόσθετες θεραπείες που διατηρούν την ουροδόχο κύστη (bladder–sparing therapies BSTs). Η ανάγκη ανάπτυξης και επικύρωσης νέων θεραπευτικών στρατηγικών για αυτόν τον απαιτητικό πληθυσμό κρίνεται απαραίτητη. Τέτοιες αναδυόμενες θεραπευτικές προσεγγίσεις περιλαμβάνουν:
- αναστολείς σημείων ελέγχου του ανοσοποιητικού (immune checkpoint inhibitors, ICIs),
- ογκολυτικές ιογενείς θεραπείες,
- προηγμένα συστήματα ενδοκυστικής χορήγησης φαρμάκων και
- στοχευμένους μοριακούς παράγοντες.
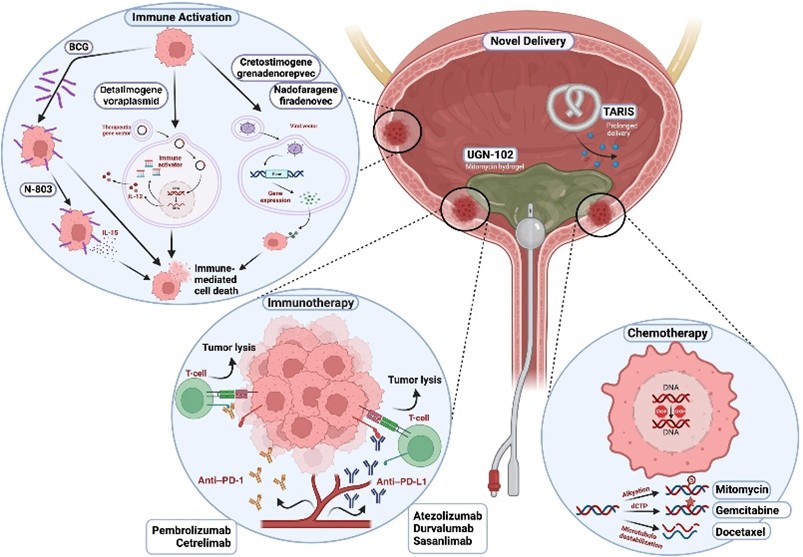
Εξατομικευμένη μοριακή θεραπεία σε υψηλού κινδύνου ασθενείς με καρκίνο της ουροδόχου κύστης
Οι πρόσφατες θεραπευτικές εξελίξεις, συμπεριλαμβανομένων της προσθήκης της ανοσοθεραπείας στην πρώτης γραμμής θεραπείας αλλά και την δυνατότητα χορήγησης εξατομικευμένης μοριακής θεραπείας στους ασθενείς με καρκίνο της ουροδόχου κύστης, έχουν αναδιαμορφώσει πλήρως τα ποσοστά επιβίωσης και υποτροπών του νοσήματος.